Entendendo a demência na doença de Alzheimer: sintomas, diagnóstico e tratamento
Entender sobre a demência na doença de Alzheimer é fundamental para lidar com esta doença neurodegenerativa complexa que afeta milhões de pessoas globalmente.
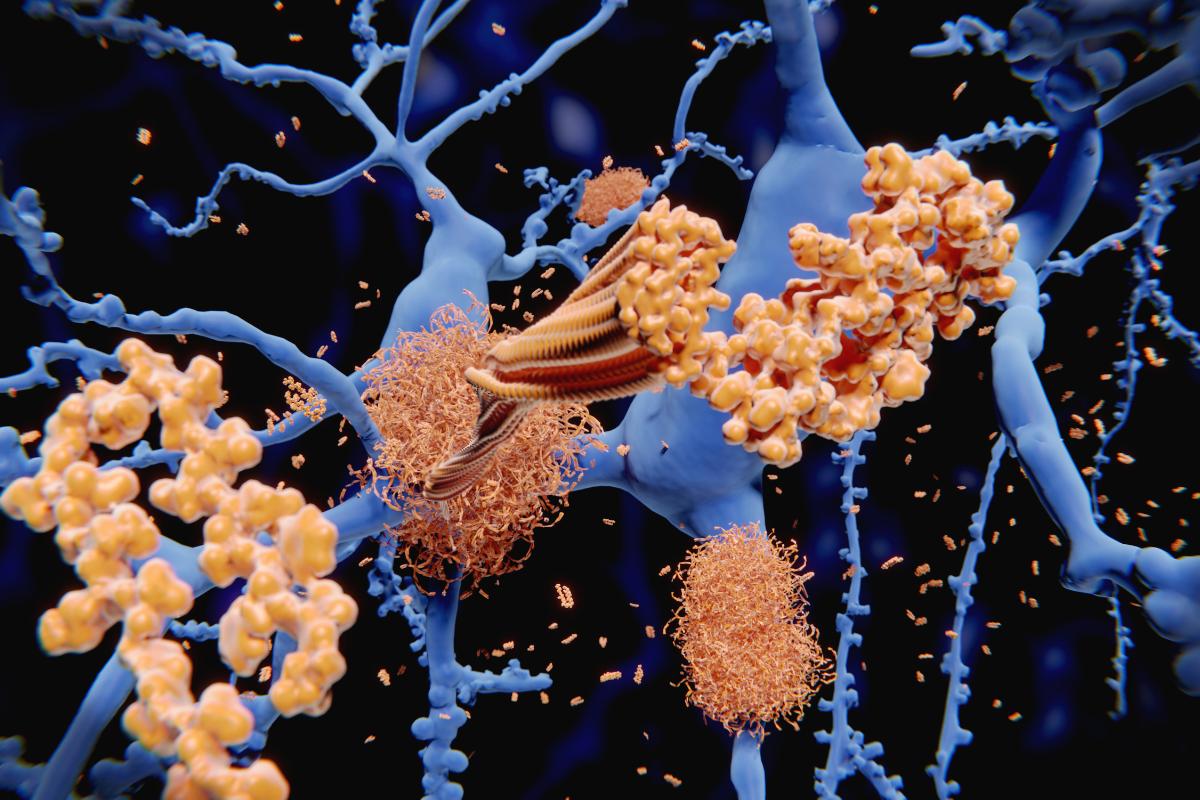
Esta condição leva a deterioração progressiva das funções cognitivas, como memória e linguagem, devido ao acúmulo de placas de proteína beta-amilóide e formação de emaranhados neurofibrilares de proteína tau no cérebro.
Diagnosticar precocemente é importante para iniciar tratamentos que podem melhorar a qualidade de vida dos pacientes.
A pesquisa atual concentra-se em novos medicamentos, avanços em tecnologias de imagem e estratégias de cuidado não farmacológicas.
Compreender esses aspectos não apenas ajuda no manejo da doença, mas também oferece esperança através de terapias mais eficazes e personalizadas.
História da demência de Alzheimer
A história da demência de Alzheimer remonta ao início do século XX, quando o médico alemão Alois Alzheimer descreveu pela primeira vez a condição em uma paciente de 51 anos. Ele observou um quadro demencial clinicamente caracterizado por mudanças progressivas profundas no comportamento e na memória da paciente, que faleceu em 1906. Ao examinar seu cérebro post-mortem, o Dr. Alzheimer identificou um cérebro com uma doença com características distintas, como placas e emaranhados anormais.
Desde então, pesquisadores têm continuado a investigar e compreender melhor a doença. Nos anos subsequentes, estudos adicionais expandiram o conhecimento sobre os mecanismos neuropatológicos que levam à demência de Alzheimer, incluindo o papel das proteínas beta-amilóide e tau na degeneração neuronal.
A descoberta de genes associados à demência na doença de Alzheimer nas décadas de 1990 e 2000 trouxe novas informações sobre os fatores genéticos predisponentes à doença. Esses avanços permitiram o desenvolvimento de testes genéticos e abriram caminho para estudos mais direcionados sobre prevenção e tratamento.
Atualmente, a história do conhecimento sobre a demência na doença de Alzheimer continua a evoluir com avanços significativos em neuroimagem, biomarcadores e terapias experimentais.
A compreensão cada vez maior da complexidade da doença impulsiona a busca por intervenções mais eficazes e estratégias preventivas para enfrentar este desafio crescente de saúde pública global.
O que é a demência na doença de Alzheimer e sua importância médica?
A demência na doença de Alzheimer - comumente chamada de demência de Alzheimer - é uma doença neurodegenerativa que afeta principalmente idosos, caracterizada por perda da capacidade funcional devido ao declínio progressivo nas funções cognitivas, como memória e linguagem.
A doença de Alzheimer, por sua vez, é o conjunto de alterações biológicas no tecido cerebral caracterizado pelo acúmulo anormal de placas de proteína beta-amilóide e pela formação de emaranhados neurofibrilares no cérebro, resultando na perda gradual de células nervosas que leva progressivamente ao quadro demencial.
A importância médica da demência de Alzheimer é extremamente significativa devido à sua crescente prevalência global, representando um desafio substancial para pacientes, cuidadores e sistemas de saúde.
Diagnosticar a doença precocemente é crucial para iniciar intervenções terapêuticas e de suporte adequadas, que não apenas ajudam a retardar a progressão da doença, mas também melhoram significativamente a qualidade de vida dos afetados.
Atualmente, a pesquisa está intensamente focada no desenvolvimento de tratamentos mais eficazes e estratégias preventivas para enfrentar esse problema de saúde pública crescente.
Compreender continuamente os mecanismos subjacentes à demência de Alzheimer é essencial para avançar no diagnóstico precoce e no manejo da doença, oferecendo esperança para o futuro na luta contra essa condição incapacitante.
Investimentos significativos em pesquisa estão sendo feitos para identificar biomarcadores precoces, explorar novas terapias farmacológicas e não farmacológicas, e investigar fatores genéticos e ambientais que podem influenciar o desenvolvimento da doença.
Esses esforços são essenciais para encontrar soluções eficazes que possam fazer uma diferença tangível na vida dos pacientes e suas famílias.
Sobre a demência de Alzheimer
A demência de Alzheimer é uma condição cerebral progressiva e irreversível que afeta mais de 6,5 milhões de americanos com 65 anos ou mais. Essa condição gradualmente compromete a memória, as habilidades de pensamento e, progressivamente, a capacidade de realizar tarefas simples, tornando-se a forma mais comum de demência entre os idosos e uma preocupação significativa de saúde pública.
Embora as causas específicas da doença de Alzheimer não sejam totalmente conhecidas, atualmente a ciência considera que a doença deve-se essencialmente ao acúmulo de placas beta-amilóides e, consequentemente, à formação de emaranhados neurofibrilares de proteína tau no cérebro.
Essas alterações resultam na perda de neurônios e suas conexões, impactando severamente a capacidade de lembrar, pensar e se comunicar. À medida que avança, os sintomas se intensificam, levando à necessidade de assistência completa.
Inicialmente, a doença de Alzheimer se manifesta com perda de memória recente, dificuldade em encontrar palavras e desorientação temporal. Com a progressão, surgem desorganização mental, alterações de humor e comportamento, além de dificuldades com linguagem e coordenação. Eventualmente, os pacientes perdem a capacidade de realizar atividades cotidianas e reconhecer entes queridos.
Além do impacto devastador para os pacientes, a demência de Alzheimer impõe um ônus significativo aos cuidadores e sistemas de saúde, elevando os custos e demandando cuidados especializados à medida que a doença avança. Investigações contínuas são cruciais para melhorar o entendimento da doença e desenvolver tratamentos mais eficazes e estratégias preventivas.
A educação e conscientização sobre a doença de Alzheimer são essenciais para diagnóstico precoce e manejo adequado, promovendo melhor qualidade de vida para todos afetados.
Epidemiologia da demência de Alzheimer
A epidemiologia da demência de Alzheimer revela-se uma preocupação crescente à medida que a população global envelhece. Estima-se que mais de 50 milhões de pessoas em todo o mundo vivam com demência de Alzheimer ou outra forma de demência, e esse número deve quase triplicar até 2050. A prevalência de demência varia significativamente por região e está intimamente ligada ao aumento da expectativa de vida.
Nos Estados Unidos, por exemplo, cerca de 6 milhões de pessoas têm demência de Alzheimer, e esse número continua a aumentar. Na Europa, a doença afeta aproximadamente 10 milhões de indivíduos, enquanto na Ásia a prevalência também está em ascensão devido ao envelhecimento populacional e mudanças no estilo de vida.
A incidência de demência de Alzheimer é maior em idosos, com a idade sendo o principal fator de risco. Ainda assim, casos diagnosticados em pessoas mais jovens, embora mais raros, indicam uma variedade na apresentação da doença.
O crescente ônus social e econômico da demência de Alzheimer aumenta a necessidade urgente de políticas de saúde pública que apoiem diagnósticos precoces, cuidados integrados e pesquisa contínua para tratamentos mais eficazes.
Essa compreensão epidemiológica é fundamental para orientar estratégias de prevenção e manejo da doença, garantindo melhores cuidados e qualidade de vida para pacientes e suas famílias.
Anatomia, histologia e fisiologia do cérebro
A anatomia, histologia e fisiologia do cérebro são fundamentais para entender a demência na doença de Alzheimer.
O cérebro humano é dividido em áreas que se conectam e desempenham funções complexas e relativamente específicas, como memória, linguagem e movimento. A camada externa, o córtex cerebral, é essencial para processos cognitivos complexos. As células nervosas, ou neurônios, transmitem sinais eletroquímicos através de conexões chamadas sinapses.
A comunicação entre neurônios é mediada por neurotransmissores, que desempenham um papel fundamental na transmissão de informações.
No contexto da doença de Alzheimer, mudanças patológicas afetam essas estruturas e processos. A acumulação de placas de proteína beta-amilóide e formação de emaranhados neurofibrilares interferem na função normal dos neurônios, levando à degeneração e morte celular.
Além do córtex cerebral, regiões como o hipocampo, crucial para a formação de novas memórias, são especialmente vulneráveis à doença de Alzheimer. O entendimento detalhado da anatomia, histologia e fisiologia do cérebro não apenas ajuda na compreensão dos sintomas da doença, mas também orienta a pesquisa de novas terapias e estratégias preventivas.
O conhecimento dessa base anatomopatológica e histofisiopatológica é essencial para a aplicação e o desenvolvimento de abordagens eficazes de diagnóstico e tratamento, visando mitigar o impacto devastador da doença de Alzheimer no funcionamento cerebral e na qualidade de vida dos pacientes.
Fatores de risco para a demência de Alzheimer
Os fatores de risco para a demência de Alzheimer abrangem uma variedade de influências genéticas e ambientais. A idade avançada é o principal fator, pois o risco de desenvolver a doença aumenta significativamente após os 65 anos. Histórico familiar também desempenha um papel importante, com estudos sugerindo que certas variantes genéticas podem aumentar a predisposição - a exemplo do gene ApoE ε4.
Estilo de vida desempenha um papel importante; por exemplo, uma dieta rica em antioxidantes e ácidos graxos ômega-3 pode ajudar a proteger contra a demência de Alzheimer. Além disso, atividade física regular e estimulação mental estão associadas a um menor risco.
Condições de saúde como hipertensão arterial, diabetes e obesidade também podem aumentar a vulnerabilidade à demência de Alzheimer, sugerindo uma ligação entre saúde cardiovascular e saúde cerebral.
Fatores ambientais como exposição a metais pesados e toxinas podem desempenhar um papel, com pesquisas em andamento.
Compreender esses fatores de risco é crucial para orientar estratégias de prevenção. A promoção de hábitos de vida saudáveis, a monitorização de condições de saúde e o manejo de fatores de risco podem ajudar a reduzir a incidência da demência de Alzheimer e melhorar a saúde cerebral a longo prazo.
Diagnóstico precoce
O diagnóstico precoce é importante na doença de Alzheimer porque permite o início imediato de tratamentos que podem retardar a progressão da doença e melhorar a qualidade de vida do paciente.
Testes neuropsicológicos, que avaliam habilidades cognitivas como memória, linguagem e raciocínio, são fundamentais para detectar mudanças sutis que podem indicar transtorno neurocognitivo associado à doença de Alzheimer em seus estágios iniciais.
Avaliações clínicas detalhadas, incluindo histórico médico completo e exames físicos, ajudam a descartar outras condições que podem causar sintomas semelhantes.
Novas técnicas de exames de imagem cerebral, como tomografia por emissão de pósitrons (PET) e ressonância magnética funcional (fMRI), também são utilizadas para detectar alterações no cérebro associadas à doença de Alzheimer antes mesmo do aparecimento dos sintomas evidentes.
Mais recentemente, novas opções de exames com maior sensibilidade e especificidade têm sido incorporadas para fornecer com maior precisão o diagnóstico da doença de Alzheimer:
- PET-CT cerebral com marcador beta-amilóide: Utiliza imagens cerebrais para identificar depósitos de proteína beta-amilóide no cérebro, que são indicativos da doença.
- Líquido Cefalorraquidiano (LCR): Coletado em geral através de punção lombar, o LCR é analisado para detectar níveis anormais de proteínas beta-amilóide e tau.
- Exame de Sangue (tau-fosforilada 217, razão beta-amilóide 42/40, APS2): Avalia biomarcadores específicos no sangue que ajudam a identificar a presença da doença de Alzheimer.
Patologia da doença de Alzheimer
A patologia da doença de Alzheimer envolve mudanças complexas no cérebro que afetam diretamente a função cognitiva. A característica principal é o acúmulo de placas de proteína beta-amilóide entre os neurônios. Essas placas interferem na comunicação neuronal e contribuem para a morte celular.
Além das placas, há também a formação de emaranhados neurofibrilares dentro dos neurônios. Esses emaranhados são compostos por uma proteína chamada tau - que perde sua estrutura normal - e se agrupam anormalmente, causando disfunção celular adicional.
Essas alterações patológicas resultam na perda progressiva de conexões neuronais e na degeneração dos próprios neurônios, especialmente em áreas do cérebro responsáveis pela memória e outras funções cognitivas. A neuroinflamação crônica também é observada no cérebro de pacientes com demência de Alzheimer, contribuindo para o ciclo de danos celulares e neurodegeneração.
A compreensão detalhada desses processos é crucial para o desenvolvimento de tratamentos eficazes que possam interferir na progressão da doença.
Pesquisas atuais estão focadas em terapias que possam reduzir a formação de placas beta-amilóide e emaranhados neurofibrilares, bem como abordagens que visam a proteção neuronal e a redução da inflamação cerebral.
Essa visão da neuropatologia da doença de Alzheimer ajuda a elucidar os mecanismos biológicos subjacentes à demência e a orientar esforços contínuos para encontrar estratégias terapêuticas que possam melhorar a qualidade de vida dos pacientes afetados.
Sintomas iniciais da demência de Alzheimer
Os sintomas iniciais da demência de Alzheimer podem ser sutis e facilmente atribuídos ao envelhecimento normal. A perda de memória recente é frequentemente uma das primeiras manifestações, como esquecer eventos recentes ou repetir perguntas. Dificuldades em planejar ou resolver problemas simples também podem surgir, além de prejuízo na capacidade de realizar tarefas habituais.
À medida que a doença progride, os sintomas tornam-se mais evidentes. Desorientação sobre tempo e lugar é comum, assim como dificuldades na compreensão de imagens visuais e relacionamento de objetos. Problemas de linguagem, como substituir termos incorretamente ou dificuldade em encontrar palavras certas, são outros indicativos.
Além dos sintomas cognitivos, mudanças de humor e personalidade podem ocorrer, incluindo apatia, irritabilidade e ansiedade. À medida que a demência avança, a capacidade de realizar atividades diárias pode ser significativamente comprometida.
É fundamental reconhecer os sinais precoces para buscar avaliação médica especializada. Um diagnóstico precoce permite o início de intervenções adequadas, como terapias farmacológicas e não farmacológicas, que podem ajudar a retardar a progressão dos sintomas e melhorar a qualidade de vida do paciente e de seus cuidadores.
A conscientização sobre os sintomas iniciais do transtorno neurocognitivo associado à doença de Alzheimer não só promove uma intervenção mais adequada, mas também destaca a importância de cuidados preventivos e da pesquisa contínua para entender melhor e tratar esta doença neurodegenerativa complexa.
Variações dos sintomas
Os sintomas iniciais da doença de Alzheimer podem variar amplamente de pessoa para pessoa, mas dois aspectos adicionais importantes a serem considerados são:
- Problemas de orientação: indivíduos podem começar a apresentar dificuldades em se orientar no tempo e no espaço. Isso pode se manifestar através de confusão sobre datas, estações do ano ou até mesmo onde estão localizados em momentos específicos.
- Prejuízo na tomada de decisões: outro sintoma precoce inclui dificuldades na tomada de decisões simples do dia a dia. Isso pode ser observado em situações como escolher roupas apropriadas para o clima ou decidir o que comer em uma refeição, evidenciando um declínio gradual na capacidade de realizar tarefas cotidianas de forma autônoma.
Reconhecer esses sinais adicionais pode ajudar na identificação precoce da doença de Alzheimer, facilitando intervenções que podem ajudar a retardar sua progressão e melhorar a qualidade de vida do paciente.
Progressão dos sintomas
A progressão dos sintomas da demência de Alzheimer varia de pessoa para pessoa, mas segue um padrão geral de deterioração gradual das funções cognitivas e comportamentais.
Inicialmente, sintomas leves como esquecimento ocasional e dificuldade em encontrar palavras podem surgir. Com o tempo, problemas de memória se agravam, afetando a capacidade de recordar eventos recentes e reconhecer pessoas próximas.
À medida que a doença progride para estágios mais avançados, outras habilidades cognitivas são afetadas. A linguagem pode deteriorar-se significativamente, levando a dificuldades na comunicação verbal. Além disso, habilidades motoras podem ser comprometidas, tornando difícil realizar tarefas simples do dia a dia.
Os sintomas comportamentais também se intensificam com o tempo. Pacientes podem apresentar mudanças de humor mais frequentes e imprevisíveis, como irritabilidade, agitação ou apatia.
Com a progressão da demência, é comum observar desorientação espacial e temporal mais pronunciada, além de necessidade crescente de assistência para atividades básicas como alimentação e higiene pessoal.
Entender a progressão gradual da demência de Alzheimer é fundamental para planejar cuidados e suporte adequados ao longo do tempo. Isso inclui ajustes na rotina diária, implementação de estratégias para manter a segurança do paciente e garantir que suas necessidades médicas e emocionais sejam atendidas de maneira compassiva e eficaz.
Estágios da progressão
A demência de Alzheimer progride tipicamente por três estágios principais: inicial, intermediário e avançado. Cada estágio apresenta sintomas específicos que afetam progressivamente a capacidade cognitiva, funcional e comportamental do paciente.
Variações da demência de Alzheimer
- Demência de Alzheimer esporádica: Este é o tipo mais comum de demência de Alzheimer, representando até 95% dos casos. Não há um padrão genético claro e é geralmente atribuído a uma combinação de fatores genéticos e ambientais.
A idade de início pode variar, mas geralmente ocorre após os 65 anos. Os sintomas desenvolvem-se gradualmente ao longo do tempo, afetando a memória, linguagem e outras funções cognitivas.
- Demência de Alzheimer familiar ou genética: Este tipo é menos comum, representando aproximadamente 5% dos casos. Em geral, é herdado de forma dominante e tende a se manifestar em idades mais jovens, por volta dos 30 aos 60 anos.
É causado por mutações genéticas específicas, como nos genes APP, PSEN1 e PSEN2. Pessoas com histórico familiar positivo têm um risco maior de desenvolver a doença em comparação com a população em geral.
- Demência de Alzheimer precoce: Também conhecido como demência de Alzheimer de início precoce ou de início antes dos 65 anos, este tipo afeta indivíduos mais jovens.
É menos comum e pode estar associado a variantes genéticas específicas que causam a doença em idades mais jovens do que a demência de Alzheimer tardia.
- Demência de Alzheimer tardia: É o tipo mais comum de demência de Alzheimer e geralmente afeta pessoas acima de 65 anos. A idade avançada é o principal fator de risco, e o desenvolvimento da doença está frequentemente relacionado a fatores como idade, histórico familiar e condições de saúde geral.
Compreender essas diferentes apresentações da demência de Alzheimer é crucial para diagnósticos precisos e para orientar estratégias de tratamento e cuidado personalizadas para cada paciente.
Diagnóstico de demência associada à doença de Alzheimer
O diagnóstico de transtorno neurocognitivo associado à doença de Alzheimer envolve uma avaliação abrangente baseada em sintomas observados e testes clínicos. Inicialmente, o médico realiza uma história clínica detalhada para entender os sintomas e seu impacto na vida diária do paciente. Testes cognitivos são aplicados para avaliar funções como memória, linguagem e habilidades de pensamento.
Exames de imagem, como tomografia computadorizada (TC) ou ressonância magnética (RM) de crânio, ajudam a excluir outras causas possíveis dos sintomas e a avaliar mudanças estruturais no cérebro. Biomarcadores no líquido cefalorraquidiano (LCR) , em exame de sangue ou imagens de PET-CT cerebral com marcador beta-amilóide podem ser utilizados para detecção de anormalidades associadas a placas de beta-amilóide e emaranhados neurofibrilares.
O diagnóstico diferencial é essencial para distinguir a doença de Alzheimer de outras condições que podem apresentar sintomas semelhantes, como depressão ou déficits vitamínicos. Uma equipe multidisciplinar, incluindo neurologistas, psiquiatras e neuropsicólogos, muitas vezes colabora para obter um diagnóstico preciso.
Um diagnóstico precoce é fundamental para iniciar intervenções que podem ajudar a retardar a progressão da doença e melhorar a qualidade de vida do paciente. Sendo assim, permite que pacientes e familiares planejem adequadamente o futuro e aproveitem ao máximo os recursos disponíveis.
Entender o processo diagnóstico da doença de Alzheimer é crucial para promover uma abordagem holística e integrativa no cuidado de pacientes, proporcionando suporte integral e personalizado ao longo da jornada da doença.
Tratamentos atuais para demência de Alzheimer
- Medicamentos para sintomas cognitivos: Inibidores da colinesterase, como donepezila, rivastigmina e galantamina, são comumente prescritos para adiar a progressão do prejuízo de funções cognitivas, como memória, linguagem e pensamento.
Eles funcionam aumentando os níveis de acetilcolina, um neurotransmissor crucial para a comunicação entre neurônios no cérebro afetado pela doença de Alzheimer.
- Medicamentos para sintomas comportamentais: Em casos nos quais sintomas como agitação, ansiedade, irritabilidade ou agressividade são proeminentes, podem ser utilizados antidepressivos, antipsicóticos ou estabilizadores de humor a critério médico.
Estes medicamentos ajudam a regular o humor e reduzir comportamentos disruptivos, proporcionando maior conforto ao paciente e melhorando a interação com cuidadores e familiares.
- Terapias não farmacológicas: Terapias comportamentais focam em manter as habilidades funcionais do paciente, promovendo independência em atividades diárias.
Fisioterapia pode ajudar a manter a mobilidade e prevenir complicações decorrentes da imobilidade. A musicoterapia, por sua vez, utiliza música para estimular áreas do cérebro relacionadas à memória e emoção, oferecendo conforto e bem-estar ao paciente.
- Abordagens baseadas em estilo de vida: Estimulação cognitiva através de jogos, quebra-cabeças e atividades que desafiam o cérebro podem ajudar a preservar funções cognitivas e retardar o declínio, mas ainda há pesquisas em andamento.
Atividades sociais regulares também são benéficas, pois promovem interações sociais que são importantes para o bem-estar emocional e mental.
- Cuidados de apoio: Além do tratamento direto ao paciente, é essencial fornecer apoio emocional aos cuidadores e familiares, que desempenham um papel fundamental no manejo diário da doença.
Programas de suporte, como grupos de apoio e educação sobre a demência de Alzheimer, ajudam a proporcionar um ambiente de cuidado mais informado e solidário.
Aprovação de anticorpos monoclonais pela FDA
A Food and Drug Administration (FDA) dos EUA recentemente concedeu aprovação à infusão dos anticorpos monoclonais lecanemabe e donanemabe para o tratamento da doença de Alzheimer. Este marco representa uma nova esperança para pacientes com comprometimento cognitivo leve ou estágio inicial de demência associados à doença de Alzheimer, os grupos foco dos ensaios clínicos.
O donanemabe é administrado como uma infusão intravenosa a cada quatro semanas. A dosagem recomendada é detalhada nas informações de prescrição, com um regime inicial de 700 mg a cada 4 semanas para as primeiras três doses, seguido por 1400 mg a cada 4 semanas.
A aprovação do donanemabe pela FDA é baseada em evidências de eficácia e segurança. Em um estudo duplo-cego, controlado por placebo (Estudo 1, NCT04437511), 1736 pacientes foram randomizados para receber donanemabe ou placebo por até 72 semanas.
Pacientes tratados com donanemabe demonstraram uma redução estatisticamente significativa no declínio clínico na Escala Integrada de Avaliação da Doença de Alzheimer (iADRS) em comparação com o placebo na Semana 76. Além disso, melhorias foram observadas na subescala cognitiva ADAS-Cog13 e na escala ADCS-iADL.
A segurança do donanemabe foi cuidadosamente avaliada. As informações do fabricante incluem um alerta para anormalidades de imagem relacionadas à amilóide (ARIA), que pode se apresentar como edema (inchaço) temporário no cérebro ou pequenos pontos de sangramento. Pacientes homozigotos do gene ApoE ε4 têm maior incidência de ARIA, sugerindo a necessidade de teste genético antes do início do tratamento.
Além disso, há risco de reações relacionadas à infusão, como sintomas semelhantes a gripe, náuseas, vômitos e alterações na pressão arterial. Reações de hipersensibilidade, incluindo anafilaxia e angioedema, também foram reportadas. Os efeitos colaterais mais comuns foram ARIA e dor de cabeça.
A FDA concedeu ao donanemabe designações de “Fast Track", "Priority Review" e "Breakthrough Therapy", refletindo a urgência e a promessa desse tratamento inovador na luta contra a doença de Alzheimer.
Administração e dosagem do donanemabe
O donanemabe é administrado por infusão intravenosa a cada quatro semanas, conforme detalhado nas informações do fabricante para garantir sua eficácia e segurança.
Os pacientes inicialmente recebem 700 mg nas primeiras três doses, seguidos por 1400 mg a cada quatro semanas. Este protocolo foi estabelecido com base em estudos clínicos rigorosos que avaliaram a resposta dos pacientes e sua tolerância ao medicamento.
É fundamental que os pacientes sigam rigorosamente o cronograma de dosagem recomendado e realizem as infusões sob supervisão médica para monitorar possíveis reações adversas e ajustar o tratamento conforme necessário.
Cuidados e manejo da doença
Cuidar de alguém com demência de Alzheimer requer uma abordagem holística e integrativa para garantir conforto e qualidade de vida. Isso inclui:
- Ambiente seguro: Modificar a casa pode incluir a instalação de corrimãos, barras de apoio no banheiro e iluminação adequada para reduzir o risco de quedas. Remover objetos desnecessários ou potencialmente confusos ajuda a manter o ambiente claro e organizado.
- Rotina estruturada: Estabelecer horários fixos para refeições, atividades e descanso ajuda a reduzir a ansiedade do paciente, proporcionando previsibilidade. Isso também pode incluir horários para medicação e atividades de lazer.
- Comunicação clara: Utilizar linguagem simples e direta, com frases curtas e pausas para permitir que o paciente processe informações. Evitar conversas complexas ou ambíguas ajuda a minimizar a frustração e a confusão.
- Estímulo cognitivo: Atividades como quebra-cabeças, jogos de memória e leitura podem ajudar a manter as habilidades cognitivas. Música e arte também são formas eficazes de estimular o cérebro e promover o bem-estar emocional.
- Nutrição adequada: Uma dieta balanceada, rica em frutas, vegetais, grãos integrais e proteínas magras, é fundamental. Incentivar a hidratação regular também é importante para a saúde geral e o funcionamento cognitivo.
- Suporte emocional: Tanto o paciente quanto os cuidadores podem se beneficiar de grupos de apoio, onde compartilham experiências e aprendem estratégias de enfrentamento. Educação sobre a doença ajuda a reduzir o estigma e a aumentar o entendimento sobre os desafios enfrentados.
- Monitoramento médico: Consultas regulares com profissionais de saúde permitem ajustes no tratamento conforme necessário. Avaliações periódicas ajudam a monitorar a progressão da doença e a adaptar o plano de cuidados de acordo.
Implementar essas práticas não apenas melhora a qualidade de vida do paciente com demência de Alzheimer, mas também apoia os cuidadores, proporcionando-lhes recursos e estratégias para enfrentar os desafios diários da doença.
Impacto social e econômico da demência de Alzheimer
O impacto da demência de Alzheimer na sociedade abrange diversas áreas cruciais:
O impacto social da doença é profundo, afetando não apenas os pacientes, mas também suas famílias. Cuidadores enfrentam desafios emocionais e físicos significativos, muitas vezes resultando em isolamento social e estresse emocional. A progressiva necessidade de cuidados intensos pode impactar negativamente a dinâmica familiar e a qualidade de vida de todos os envolvidos.
Em termos econômicos, a demência de Alzheimer gera custos substanciais. Os gastos diretos com cuidados médicos e os indiretos, como perda de produtividade no trabalho e necessidade de cuidadores, representam um fardo significativo para os sistemas de saúde e economias individuais. Esses custos tendem a aumentar à medida que a doença progride e mais cuidados especializados são necessários.
No âmbito educativo, a conscientização sobre a demência de Alzheimer é essencial. A falta de entendimento sobre a doença pode levar a estigmas sociais e dificultar o acesso a recursos adequados. A educação da população sobre os sintomas, cuidados e suporte disponível é crucial para melhorar a qualidade de vida dos pacientes e cuidadores.
Investimentos em pesquisa são fundamentais para avançar no entendimento da demência de Alzheimer e desenvolver tratamentos eficazes. Avanços científicos podem não apenas retardar a progressão da doença, mas também melhorar a qualidade de vida dos afetados e reduzir os custos associados ao seu manejo.
Em um nível político, políticas públicas voltadas para apoiar cuidadores, promover acesso a serviços de saúde e incentivar a pesquisa são indispensáveis. A implementação de políticas que reconheçam e respondam às necessidades das pessoas com demência de Alzheimer e suas famílias é importante para mitigar o impacto da doença na sociedade.
Apoio psicológico e emocional
O apoio psicológico e emocional desempenha um papel crucial na jornada de pacientes e familiares enfrentando a demência de Alzheimer:
É fundamental proporcionar um espaço seguro para que pacientes e familiares possam expressar emoções complexas como tristeza, frustração e ansiedade. Isso não apenas alivia o estresse emocional, mas também fortalece o bem-estar geral.
Os grupos de apoio desempenham um papel valioso, pois oferecem uma comunidade de indivíduos que compartilham experiências semelhantes. Esses grupos permitem que pessoas em situações semelhantes se conectem, compartilhem informações e ofereçam apoio mútuo, proporcionando um senso de companheirismo e compreensão.
A psicoterapia individual é uma ferramenta essencial que oferece não apenas um espaço seguro para explorar emoções, mas também estratégias práticas para lidar com o impacto emocional da doença. Os pacientes e cuidadores podem aprender técnicas para enfrentar desafios específicos e desenvolver habilidades de enfrentamento eficazes.
Educar familiares e cuidadores sobre as mudanças comportamentais e cognitivas associadas à demência de Alzheimer é crucial. Isso não só melhora a compreensão das dificuldades enfrentadas pelo paciente, mas também equipa os cuidadores com conhecimentos práticos para lidar com situações desafiadoras de maneira mais eficaz e empática.
Oferecer suporte contínuo aos cuidadores é essencial para ajudá-los a manter um equilíbrio saudável entre cuidar de si mesmos e cuidar do paciente. Isso pode incluir acesso a orientação sobre cuidados pessoais e monitoramento do bem-estar emocional dos cuidadores.
Esse suporte integral não apenas beneficia diretamente os pacientes e cuidadores, mas também contribui para uma qualidade de vida melhor e mais sustentável ao longo do curso da doença.
Pesquisa e avanços futuros
A pesquisa sobre doença de Alzheimer está na vanguarda da medicina atual, concentrando-se em diversas áreas essenciais que podem revolucionar o tratamento e manejo da doença.
Novos medicamentos estão sendo rigorosamente estudados para modificar a progressão da doença de Alzheimer, visando destruir proteínas anômalas e evitar a progressão de placas de beta-amilóide no cérebro afetado.
Avanços significativos em tecnologias de imagem, como PET e ressonância magnética funcional, estão possibilitando uma visualização mais detalhada e precisa das mudanças estruturais e funcionais no cérebro de pacientes com Alzheimer. Essas tecnologias são fundamentais para o suporte diagnóstico precoce e acompanhamento da progressão da doença.
Novas pesquisas têm demonstrado que testes diagnósticos mais sensíveis e específicos, tais como PET-CT cerebral com marcador beta-amilóide e biomarcadores no líquido cefalorraquidiano (LCR) ou no sangue, podem proporcionar maior precisão do diagnóstico da doença.
Estudos genéticos continuam a identificar variantes genéticas que aumentam o risco de desenvolvimento da doença de Alzheimer, permitindo estratégias de intervenção personalizadas e a identificação precoce de indivíduos em maior risco.
Além dos tratamentos farmacológicos em desenvolvimento, a pesquisa está explorando intervenções não farmacêuticas, como alimentação saudável, suplementos, exercícios físicos e programas de estimulação cognitiva. Essas abordagens têm mostrado potencial para retardar o declínio cognitivo e melhorar a qualidade de vida dos pacientes.
O financiamento global para pesquisa em doença de Alzheimer está em ascensão, incentivando colaborações multidisciplinares entre acadêmicos, indústria farmacêutica e organizações sem fins lucrativos. Essa cooperação é essencial para acelerar descobertas e traduzir pesquisas básicas em avanços clínicos significativos.
O futuro da pesquisa promete terapias mais eficazes e personalizadas, diagnósticos mais precisos e estratégias de prevenção mais robustas. Esses avanços não apenas têm o potencial de melhorar a qualidade de vida dos pacientes, mas também de aliviar o ônus sobre cuidadores e sistemas de saúde, oferecendo esperança significativa para aqueles afetados por esta doença devastadora.
Avanços no tratamento da demência na doença de Alzheimer com o Dr. Petrus Raulino
Compreender a demência na doença de Alzheimer não é apenas essencial para aqueles que enfrentam a doença, mas para toda a sociedade. Esta condição neurodegenerativa não só impacta profundamente os indivíduos afetados e seus familiares, mas também representa um desafio significativo para os sistemas de saúde em todo o mundo.
Ao longo deste blog, exploramos desde a definição e história da demência na doença de Alzheimer até os últimos avanços em pesquisa e tratamento.
É importante reconhecer a importância do diagnóstico precoce e do acompanhamento adequado, além de explorar as diversas opções terapêuticas disponíveis, tanto farmacológicas quanto não farmacológicas.
A pesquisa contínua e o desenvolvimento de novas terapias oferecem esperança para o futuro, promovendo uma melhor qualidade de vida para pacientes e suas famílias.
Para aqueles que buscam um tratamento eficaz e personalizado, marcar uma consulta com o Dr. Petrus Raulino pode ser o primeiro passo rumo a uma vida melhor.
Como médico especializado em psiquiatria, seu enfoque baseado em evidências científicas e centrado no paciente combina conhecimentos avançados de neurobiologia com um cuidado compassivo, priorizando não apenas o bem-estar emocional, mas também o monitoramento dos fatores biológicos orgânicos que influenciam no tratamento.
Continue se informando sobre condições de saúde relacionadas à psicofarmacologia no Blog do Dr. Petrus Raulino e esteja sempre atualizado sobre as melhores práticas para lidar com a demência na doença de Alzheimer e outras doenças neuropsiquiátricas.
Genoma revela sobreposição entre Esquizofrenia e Transtorno Bipolar
Por Dr. Petrus Raulino
Um estudo publicado na revista Molecular Psychiatry analisou dados de estudo de associação genômica ampla entre Esquizofrenia, Transtorno Bipolar e inteligência geral para investigar sobreposição de variantes genéticas comuns.
Esquizofrenia e Transtorno Bipolar
A Esquizofrenia e o Transtorno Bipolar são transtornos mentais mundialmente reconhecidos entre as principais causas de morbidade e mortalidade no mundo.
Embora sejam diferentes, podem eventualmente compartilhar algumas características clínicas, incluindo alterações do humor, pensamento, percepção e funcionamento social.
As manifestações clínicas desses transtornos podem ser acompanhadas por comprometimento cognitivo, embora este tenda a ser mais grave na Esquizofrenia do que no Transtorno Bipolar.
Dentre os domínios cognitivos estão funções executivas, aprendizagem verbal, velocidade de processamento e memória, bem como inteligência geral.
Evidências crescentes indicam que o risco genético para Esquizofrenia pode contribuir para o comprometimento cognitivo.
Por sua vez, a relação genética entre Transtorno Bipolar e função cognitiva ainda permanece pouco compreendida.
No estudo em questão ficou demonstrado uma sobreposição poligênica entre inteligência, Esquizofrenia e Transtorno Bipolar.
Um locus é o local fixo em um cromossomo onde está localizado determinado gene ou marcador genético.
No estudo, foram identificados 75 loci gênicos associados em conjunto com Esquizofrenia e inteligência e 12 loci gênicos associados em conjunto com Transtorno Bipolar e inteligência.
Entre os loci compartilhados, 20 foram novos loci de risco para Esquizofrenia e 4 foram novos para Transtorno Bipolar.
Ao todo, o estudo indicou que grandes frações das arquiteturas de risco genético subjacentes a Esquizofrenia, mutações genéticas e Transtorno Bipolar também influenciam a inteligência, embora de maneira diferente.
Os resultados sugeriram que a relação genética entre os três (Esquizofrenia, Transtorno Bipolar e inteligência) é mais complexa do que é expresso por suas correlações genéticas, o que pode explicar a diversidade de desempenho cognitivo entre os diferentes grupos de pacientes.
A pesquisa forneceu novos insights sobre as bases genéticas e moleculares do desempenho cognitivo alterado nesses grupos de pacientes.
Referências
Smeland, O. B., Bahrami, S., Frei, O., Shadrin, A., O’Connell, K., Savage, J., ... & Andreassen, O. A. (2020). Genome-wide analysis reveals extensive genetic overlap between schizophrenia, bipolar disorder, and intelligence. Molecular psychiatry, 25(4), 844-853.
Consortium, I. S. (2009). Common polygenic variation contributes to risk of schizophrenia that overlaps with bipolar disorder. Nature, 460(7256), 748.
Kahn, R. S., & Keefe, R. S. (2013). Schizophrenia is a cognitive illness: time for a change in focus. JAMA psychiatry, 70(10), 1107-1112.
Keshavan, M. S., Morris, D. W., Sweeney, J. A., Pearlson, G., Thaker, G., Seidman, L. J., ... & Tamminga, C. (2011). A dimensional approach to the psychosis spectrum between bipolar disorder and schizophrenia: the Schizo-Bipolar Scale. Schizophrenia research, 133(1-3), 250-254.
Simonsen, C., Sundet, K., Vaskinn, A., Birkenaes, A. B., Engh, J. A., Færden, A., ... & Andreassen, O. A. (2011). Neurocognitive dysfunction in bipolar and schizophrenia spectrum disorders depends on history of psychosis rather than diagnostic group. Schizophrenia bulletin, 37(1), 73-83.
Keefe, R. S., & Fenton, W. S. (2007). How should DSM-V criteria for schizophrenia include cognitive impairment?. Schizophrenia bulletin, 33(4), 912-920.
Green, M. F. (2006). Cognitive impairment and functional outcome in schizophrenia and bipolar disorder. Journal of Clinical Psychiatry, 67, 3.
Desfechos psiquiátricos e neurológicos em 236.379 sobreviventes de COVID-19
Por Dr. Petrus Raulino
Desde o início da pandemia de COVID-19 é crescente a preocupação de que os sobreviventes possam ter maior risco de doenças neurológicas e psiquiátricas.
Um estudo observacional com 62.354 sobreviventes de COVID-19 demonstrou aumento do risco de transtornos de humor e ansiedade nos primeiros três meses após a infecção. Inclusive entre pacientes sem qualquer histórico psiquiátrico.
Com o passar do tempo, novas pesquisas têm contribuído para que a ciência avance ainda mais no entendimento da evolução da COVID-19.
Surgem pesquisas publicadas com dados em larga escala examinando os riscos de diagnósticos neurológicos e psiquiátricos após seis meses da infecção por COVID-19.
Novo estudo sobre condição psiquiátrica após COVID-19
Um estudo realizado recentemente na Universidade de Oxford e publicado no periódico The Lancet Psychiatry evidenciou que uma em cada três pessoas que sobreviveram à COVID-19 é diagnosticada com uma condição neurológica ou psiquiátrica seis meses após ser infectada.
Para chegar à essa conclusão, o estudo analisou os registros de saúde de mais de 230.000 pessoas com COVID-19 confirmada em 62 organizações de cuidados à saúde, principalmente dos EUA.
Resultados do estudo
No geral, a incidência estimada de diagnóstico de um transtorno neurológico ou psiquiátrico após a infecção por COVID-19 foi de 34%. Para 13% dessas pessoas, foi o primeiro diagnóstico neurológico ou psiquiátrico registrado.
Os diagnósticos mais comuns após COVID-19 foram transtornos de ansiedade (ocorrendo em 17% dos pacientes), transtornos do humor (14%), transtornos por uso de substâncias (7%) e insônia (5%).
A incidência de desfechos neurológicos foi menor, incluindo 0,6% para hemorragia cerebral, 2,1% para acidente vascular cerebral isquêmico e 0,7% para demência.
Vale ressaltar que essas incidências foram ainda maiores em pacientes que necessitaram de hospitalização e marcantemente maiores naqueles que necessitaram de internação em UTI ou desenvolveram encefalopatia.
Muitas pessoas se perguntam como uma doença respiratória pode causar efeitos psiquiátricos ou neurológicos, e para essa pergunta ainda não está clara a resposta sobre o mecanismo fisiopatológico exato.
Entretanto, há várias hipóteses para os mecanismos potenciais que provocam a associação entre COVID-19 e transtornos psiquiátricos e/ou dano neurológico. Incluem invasão viral do sistema nervoso central, estados hipercoaguláveis e efeitos neurais da resposta imune.
Conclusão
Infelizmente, muitos dos transtornos psiquiátricos identificados pelas pesquisas sobre COVID-19 tendem a ser crônicos ou recorrentes. Portanto, podemos antecipadamente presumir que o ônus da COVID-19 poderá estar conosco por muitos anos.
Por outro lado, as pesquisas continuam e também poderão nos trazer informações valiosas de como lidar ou sobrepujar o ônus decorrente da COVID-19.
Referências
Lee, M. H., Perl, D. P., Nair, G., Li, W., Maric, D., Murray, H., ... & Nath, A. (2021). Microvascular injury in the brains of patients with Covid-19. New England Journal of Medicine, 384(5), 481-483.
Taquet, M., Luciano, S., Geddes, J. R., & Harrison, P. J. (2021). Bidirectional associations between COVID-19 and psychiatric disorder: retrospective cohort studies of 62 354 COVID-19 cases in the USA. The Lancet Psychiatry, 8(2), 130-140.
Taquet, M., Geddes, J. R., Husain, M., & Harrison, P. J. (2021). Six-Month neurological and psychiatric outcomes in 236,379 survivors of COVID-19. The Lancet Psychiatry, April 6, published on-line.
Kreye, J., Reincke, S. M., & Prüss, H. (2020). Do cross-reactive antibodies cause neuropathology in COVID-19?. Nature Reviews Immunology, 20(11), 645-646.
Meinhardt, J., Radke, J., Dittmayer, C., Franz, J., Thomas, C., Mothes, R., ... & Heppner, F. L. (2021). Olfactory transmucosal SARS-CoV-2 invasion as a port of central nervous system entry in individuals with COVID-19. Nature neuroscience, 24(2), 168-175.
Rhea, E. M., Logsdon, A. F., Hansen, K. M., Williams, L. M., Reed, M. J., Baumann, K. K., ... & Erickson, M. A. (2021). The S1 protein of SARS-CoV-2 crosses the blood–brain barrier in mice. Nature neuroscience, 24(3), 368-378.
Panigada, M., Bottino, N., Tagliabue, P., Grasselli, G., Novembrino, C., Chantarangkul, V., ... & Tripodi, A. (2020). Hypercoagulability of COVID?19 patients in intensive care unit: a report of thromboelastography findings and other parameters of hemostasis. Journal of Thrombosis and Haemostasis, 18(7), 1738-1742.
Transtorno Bipolar e Neuroinflamação
Por Dr. Petrus Raulino
O que é o Transtorno Bipolar?
O Transtorno Bipolar é um subtipo de transtorno de humor. Afeta cerca de 2% da população mundial.
O Transtorno Bipolar é uma condição psiquiátrica caracterizada por no mínimo dois episódios de humor (depressão ou mania) ao longo da vida, sendo que pelo menos um deles deve ser de mania.
Estudos com gêmeos demonstraram que a carga genética do Transtorno Bipolar é da ordem de 70 a 80%.
Existem fortes evidências de que o risco para Transtorno Bipolar é poligênico, ou seja, ocorre por meio de um conjunto de alelos, cada qual apresentando um pequeno efeito para o risco.
Estudos genéticos têm demonstrado expressão aberrante de RNA mensageiro de genes inflamatórios em pacientes com Transtorno Bipolar e seus descendentes.
O papel da Neuroinflamação
Nos últimos anos, as pesquisas científicas têm aumentado substancialmente a compreensão do papel da neuroinflamação em transtornos psiquiátricos.
Uma pesquisa in vitro publicada na revista Stem Cell Reports buscou entender se a sinalização molecular alterada de astrócitos induzida por inflamação estava associada ao Transtorno Bipolar.
Os astrócitos são células conhecidas por participarem da cascata inflamatória dentro do cérebro. Eles são ativados por interleucina-1? (IL-1?) e outras citocinas pró-inflamatórias e, por sua vez, secretam citocinas que participam do processo de neuroinflamação.
A pesquisa comparou marcadores de inflamação em astrócitos derivados de células-tronco pluripotentes (iPSCs) gerados a partir de pacientes com Transtorno Bipolar e de indivíduos saudáveis.
Resultados da pesquisa
A resposta dos astrócitos dos pacientes com Transtorno Bipolar às citocinas pró-inflamatórias revelou um padrão particular, caracterizado pela maior expressão do gene da interleucina-6 (IL-6). Como resultado, essas células secretaram mais IL-6, o que impactou negativamente a atividade de neurônios.
Os fatores secretados pelos astrócitos desempenham um papel na regulação da atividade neuronal e, no caso do Transtorno Bipolar, a IL-6 faz a mediação pelo menos em parte entre os efeitos dos astrócitos estimulados pela inflamação e a atividade neuronal.
Estas descobertas sugerem que a IL-6 pode contribuir para alterações do funcionamento neuronal associados ao Transtorno Bipolar, abrindo novos caminhos para a pesquisa clínica.
Referências
Vadodaria, K. C., Mendes, A. P., Mei, A., Racha, V., Erikson, G., Shokhirev, M. N., ... & Gage, F. H. (2021). Altered neuronal support and inflammatory response in bipolar disorder patient-derived astrocytes. Stem Cell Reports.
Gordovez, F. J. A., & McMahon, F. J. (2020). The genetics of bipolar disorder. Molecular psychiatry, 25(3), 544-559.
Benedetti, F., Aggio, V., Pratesi, M. L., Greco, G., & Furlan, R. (2020). Neuroinflammation in bipolar depression. Frontiers in psychiatry, 11, 71.
Colombo, E., & Farina, C. (2016). Astrocytes: key regulators of neuroinflammation. Trends in immunology, 37(9), 608-620.
Craddock, N., & Sklar, P. (2013). Genetics of bipolar disorder. The Lancet, 381(9878), 1654-1662.
Edvardsen, J., Torgersen, S., Røysamb, E., Lygren, S., Skre, I., Onstad, S., & Øien, P. A. (2008). Heritability of bipolar spectrum disorders. Unity or heterogeneity?. Journal of affective disorders, 106(3), 229-240.
McGuffin, P., Rijsdijk, F., Andrew, M., Sham, P., Katz, R., & Cardno, A. (2003). The heritability of bipolar affective disorder and the genetic relationship to unipolar depression. Archives of general psychiatry, 60(5), 497-502.
Por que precisamos combater a Psicofobia?
Por Dr. Petrus Raulino
O que é Psicofobia?
Psicofobia é o preconceito ou discriminação contra pessoas com transtornos ou deficiências mentais.
Pode ocorrer em atitudes ou frases de preconceito contra pacientes psiquiátricos, doenças psiquiátricas, instituições em Psiquiatria, profissionais de saúde mental ou medicamentos psicotrópicos.
Infelizmente nos dias atuais esse preconceito parece-nos ainda grande, e o principal motivo para isso é a falta de conhecimento. O não saber traz esse estranhamento e as pessoas tendem a evitar o que não conhecem, muitas vezes com julgamentos falsos.
Como combater a Psicofobia?
O principal antídoto para enfrentar a psicofobia é popularizarmos informações de qualidade sobre transtornos mentais. Dessa forma podemos mudar a realidade da saúde mental em nosso país.
As possibilidades terapêuticas, até pouco tempo atrás, eram limitadas devido às perspectivas farmacológicas escassas e ao parco conhecimento. A família e a sociedade renegavam as pessoas com transtornos mentais.
No entanto esta triste realidade mudou: tratamentos eficazes, com possibilidades terapêuticas abrangentes, melhoraram o prognóstico e qualidade de vida dos pacientes.
Não há saúde sem saúde mental. Diga não ao preconceito.
Link recomendado
Genética de traços neuropsiquiátricos por sexo
Por Dr. Petrus Raulino
Uma pesquisa publicada na revista Biological Psychiatry analisou as diferenças genéticas subjacentes entre os sexos para entender porque o Transtorno Bipolar, a Esquizofrenia e o transtorno depressivo maior afetam homens e mulheres de modo e em graus diferentes.
Foram investigadas as diferenças sexuais na arquitetura genética de vinte traços neuropsiquiátricos e comportamentais usando estatísticas sumárias de análise de associação genômica ampla (GWAS) autossômica estratificada por sexo.
Foram usadas três abordagens complementares – incluindo estimativa de herdabilidade baseada em polimorfismo de nucleotídeo único (SNP), correlação genética e análises de heterogeneidade – para avaliar as diferenças de sexo dentro das características e entre pares de características.
A análise de associação genômica ampla identificou quase uma dúzia de polimorfismos de nucleotídeo único que diferiam entre homens e mulheres com diagnóstico de um dos três transtornos.
Os polimorfismos de nucleotídeo único são uma variação na sequência de DNA que afeta somente uma base nitrogenada – adenina (A), timina (T), citosina (C) ou guanina (G) – na sequência do genoma entre indivíduos de uma espécie ou entre pares de cromossomos de um individuo.
Em alguns casos, um polimorfismo de nucleotídeo único estava ligado apenas à doença em um sexo, enquanto em outros casos o mesmo polimorfismo de nucleotídeo único diminuía a probabilidade de desenvolver um distúrbio em um sexo enquanto a aumentava no outro.
Os genes que abrigam esses polimorfismos de nucleotídeo único foram ligados às vias de desenvolvimento vascular, imunológico e neuronal, fornecendo pistas sobre a interação entre a saúde cardiovascular e neurológica.
Embora a maioria dos efeitos genéticos para traços neuropsiquiátricos e comportamentais sejam semelhantes para homens e mulheres, os efeitos genéticos diferenciados por sexo podem ser identificados.
Nesse estudo foi evidenciado pela primeira vez que uma parte dos efeitos genéticos diferenciados por sexo é distribuída entre traços.
As diferenças entre os sexos na arquitetura genética autossômica comum dos fenótipos neuropsiquiátricos e comportamentais são pequenas e poligênicas. É improvável que expliquem por completo os atributos sexualmente diferenciados que observamos.
Serão necessários estudos adicionais, com amostras maiores, para avançar na identificação dos efeitos diferenciados por sexo para a maioria dos traços.
Mas o referido estudo tem implicações importantes para o futuro da pesquisa em diferenças sexuais.
Compreender a base biológica das diferenças sexuais nas doenças humanas, incluindo os fenótipos neuropsiquiátricos, é fundamental para o desenvolvimento de diagnósticos e terapêuticas baseados no sexo e para cumprir a meta da medicina de precisão.
Referências
Martin, J., Khramtsova, E. A., Goleva, S. B., Blokland, G. A., Traglia, M., Walters, R. K., ... & Stahl, E. (2021). Examining sex-differentiated genetic effects across neuropsychiatric and behavioral traits. Biological Psychiatry.
Khramtsova, E. A., Davis, L. K., & Stranger, B. E. (2019). The role of sex in the genomics of human complex traits. Nature Reviews Genetics, 20(3), 173-190.
Estresse traumático na infância pode levar a mudanças cerebrais na idade adulta
Por Dr. Petrus Raulino
Um estudo realizado na Universidade de Alberta mostrou que eventos traumáticos ou estressantes na infância podem afetar o volume de estruturas cerebrais. O estudo foi publicado na revista científica Journal of Psychiatry & Neuroscience.
Os eventos traumáticos na infância podem induzir a mudanças biológicas na estrutura cerebral: especialmente em sub-regiões específicas dos hipocampos e amígdalas cerebrais.
Na fase adulta, essas alterações podem tornar-se mal adaptativas, tornando as pessoas mais vulneráveis a transtornos psiquiátricos.
Sabe-se que o estresse pós-traumático é um fator de risco bem conhecido para o desenvolvimento de transtornos mentais, como o Transtorno Depressivo Maior (TDM) na idade adulta.
O hipocampo é fundamental para a formação e arquivamento de memórias emocionais e verbais. A amígdala é corresponsável pela criação de conteúdo emocional de memórias associadas a respostas agressivas e ao medo.
Para o estudo, foram recrutados 35 participantes com diagnóstico de Transtorno Depressivo Maior e 35 participantes saudáveis para grupo-controle.
Foram realizados exames de ressonância magnética de crânio. O histórico de traumas na infância foi avaliado por meio de escala (Childhood Trauma Questionnaire).
O estudo apresentou evidências in vivo de associações negativas entre história de maus tratos na infância e volumes na amígdala direita, hipocampo anterior e subcampo do corno de Amon total (CA 1-3) bilateralmente.
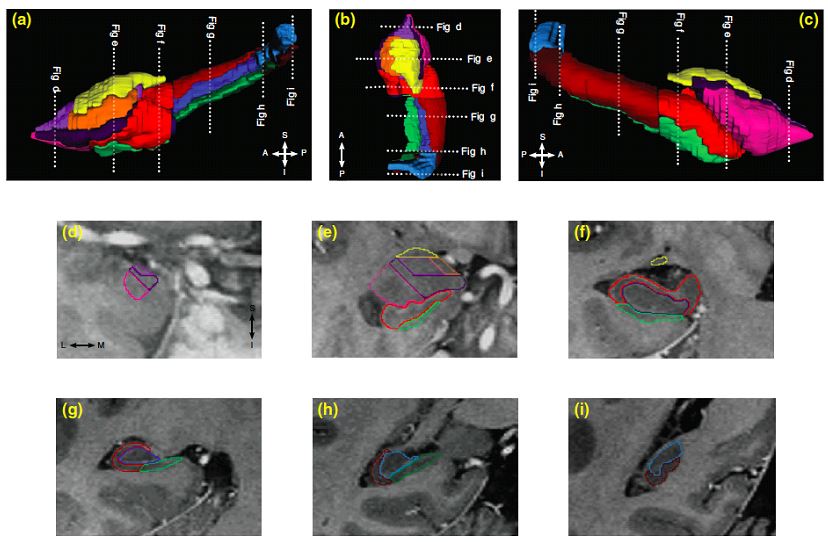
Maior escore de história de maus tratos na infância foi associado a menor volume de estruturas do lobo temporal medial em participantes com Transtorno Depressivo Maior.
Os achados da pesquisa podem representar mais um passo na direção para identificar os mecanismos biológicos potenciais pelos quais os maus tratos na infância levam a impactos clínicos na vida adulta.
Referências
Aghamohammadi-Sereshki, A., Coupland, N. J., Silverstone, P. H., Huang, Y., Hegadoren, K. M., Carter, R., ... & Malykhin, N. V. (2021). Effects of childhood adversity on the volumes of the amygdala subnuclei and hippocampal subfields in individuals with major depressive disorder. Journal of Psychiatry & Neuroscience: JPN, 46(1), E186.
Schmaal, L., Veltman, D. J., van Erp, T. G., Sämann, P. G., Frodl, T., Jahanshad, N., ... & Hibar, D. P. (2016). Subcortical brain alterations in major depressive disorder: findings from the ENIGMA Major Depressive Disorder working group. Molecular psychiatry, 21(6), 806-812.
Lindert, J., von Ehrenstein, O. S., Grashow, R., Gal, G., Braehler, E., & Weisskopf, M. G. (2014). Sexual and physical abuse in childhood is associated with depression and anxiety over the life course: systematic review and meta-analysis. International journal of public health, 59(2), 359-372.
Depressão pós-parto pode persistir três anos após o parto
Por Dr. Petrus Raulino
O que é Depressão Materna?
A depressão materna é o transtorno mental de maior prevalência durante a gestação e o puerpério.
A depressão materna contribui para prejuízos na interação com o bebê e aumenta o risco dos bebês para distúrbios cognitivos, emocionais e comportamentais.
A depressão após o parto
Um estudo publicado na revista Pediatrics conduzido por pesquisadores do Instituto Nacional de Saúde Infantil e Desenvolvimento Humano (NICHD) demonstrou que 1 a cada 4 mulheres experimentou altos níveis de sintomas depressivos em algum momento nos três anos após o parto.
Para comparação, a prevalência de depressão ao longo da vida na população geral é de cerca de 20%.
Portanto, a prevalência de 25% de depressão nos três anos seguintes ao parto é elevada e chama a atenção.
Os pesquisadores também identificaram quatro trajetórias de sintomas depressivos pós-parto e os fatores que podem aumentar os riscos de uma mulher desenvolver sintomas graves.
As trajetórias dos sintomas depressivos foram identificadas como:
- Baixo-estável, caracterizada por sintomas brandos no período (74,7%);
- Baixo-crescente, caracterizado por sintomas inicialmente brandos, mas crescentes no período (8,2%);
- Médio-decrescente, caracterizado por sintomas inicialmente moderados, mas remitidos ao longo do tempo (12,6%);
- Alto-persistente, caracterizado por sintomas em níveis elevados e persistentes (4,5%).
Perfis mais sujeitos a desenvolver sintomas depressivos no puerpério
Mulheres com história de transtornos de humor no passado ou durante a gestação são sujeitas a desenvolver sintomas depressivos no puerpério.
Gravidez não planejada ou não desejada também são fatores que aumentam o estresse e podem causar o aparecimento dos sintomas.
Fatores físicos, emocionais e de estilo de vida também podem influenciar de alguma forma o surgimento de transtorno depressivo.
Evidências sugerem que muitas mães não procuram tratamento. Muitas mulheres esperam que os sintomas passem sem tratamento.
O tratamento adequado protege a mãe e o bebê contra o ônus da depressão. É importante buscar suporte especializado em saúde mental. O conhecimento qualificado faz diferença.
Referências
Putnick, D. L., Sundaram, R., Bell, E. M., Ghassabian, A., Goldstein, R. B., Robinson, S. L., ... & Yeung, E. (2020). Trajectories of maternal postpartum depressive symptoms. Pediatrics, 146(5).
Dennis, C. L., & Chung?Lee, L. (2006). Postpartum depression help?seeking barriers and maternal treatment preferences: A qualitative systematic review. Birth, 33(4), 323-331.
Biomarcador sanguíneo pode ajudar a predizer Demência de Alzheimer anos antes que os sintomas apareçam?
Por Dr. Petrus Raulino
Um estudo publicado na revista Nature Translational Psychiatry evidenciou que idosos com proteína ácida fibrilar glial (GFAP) elevada no sangue apresentam maior acúmulo de proteína beta-amilóide no cérebro, um biomarcador associado a Demência de Alzheimer.
Mas afinal, o que é a GFAP?
A GFAP é uma proteína do citoesqueleto dos astrócitos que serve como um marcador da astrogliose – ativação e proliferação anormal de astrócitos decorrente de dano neuronal.
A proteína GFAP é encontrada no cérebro, mas pode ser medida em amostras de sangue quando o cérebro é danificado pela Demência de Alzheimer A no estágio inicial.
Atualmente, não há cura ou tratamento eficaz para reverter a Demência de Alzheimer, apesar de todos os esforços científicos. Por isso, há muitos estudos recentes buscando se concentrar em programas de prevenção e identificação de populações sob risco para Demência de Alzheimer.
Esses estudos têm reportado níveis elevados de GFAP no sangue em Demência de Alzheimer precoce e tardia. Esses níveis se correlacionam inversamente com a cognição e com a extensão da lesão da substância branca.
GFAP e os sintomas inicias da Dêmencia de Alzheimer
Mas o estudo publicado na Nature Translational Psychiatry investigou se os níveis elevados de GFAP no sangue precedem o início dos sintomas clínicos da Demência de Alzheimer em idosos cognitivamente normais sob maior risco de Demência de Alzheimer.
Resultados do estudo
A pesquisa mostrou que níveis plasmáticos de GFAP aumentados em idosos cognitivamente normais foram associados a maior acúmulo de proteína beta-amilóide no cérebro.
Portanto, o nível de GFAP plasmático aumentado pode servir como um biomarcador sanguíneo inicial para identificar indivíduos cognitivamente normais sob maior risco de Demência de Alzheimer.
Em nosso conhecimento, esse foi o primeiro estudo a demonstrar níveis plasmáticos aumentados de GFAP em idosos cognitivamente normais sob risco de Demência de Alzheimer. Essas observações sugerem que os danos se iniciam no estágio pré-sintomático da Demência de Alzheimer e está associado a acúmulo de beta-amilóide no cérebro.
Mais pesquisas são necessárias para avaliar se a dosagem de GFAP poderá fazer diferença para fundamentar estratégias de prevenção contra a Demência de Alzheimer. Por enquanto, estamos de olho em novas pesquisas.
Referências
Chatterjee, P., Pedrini, S., Stoops, E., Goozee, K., Villemagne, V. L., Asih, P. R., ... & Martins, R. N. (2021). Plasma glial fibrillary acidic protein is elevated in cognitively normal older adults at risk of Alzheimer’s disease. Translational psychiatry, 11(1), 1-10.
Elahi, F. M., Casaletto, K. B., La Joie, R., Walters, S. M., Harvey, D., Wolf, A., ... & Kramer, J. H. (2019). Plasma biomarkers of astrocytic and neuronal dysfunction in early-and late-onset Alzheimer's disease. Alzheimer's & Dementia.
Colangelo, A. M., Alberghina, L., & Papa, M. (2014). Astrogliosis as a therapeutic target for neurodegenerative diseases. Neuroscience letters, 565, 59-64.
Carter, S. F., Schöll, M., Almkvist, O., Wall, A., Engler, H., Långström, B., & Nordberg, A. (2012). Evidence for astrocytosis in prodromal Alzheimer disease provided by 11C-deuterium-L-deprenyl: a multitracer PET paradigm combining 11C-Pittsburgh compound B and 18F-FDG. Journal of Nuclear Medicine, 53(1), 37-46.
Ansiedade em homens no período perinatal
Por Dr. Petrus Raulino
Uma meta-análise publicada no periódico The Journal Psychosomatic Obstetrics & Gynecology evidenciou que a prevalência de ansiedade entre homens durante o período perinatal, que inclui a gravidez até o primeiro ano pós-parto, foi de quase 11%.
Essa taxa foi bem mais alta do que a taxa de prevalência que seria esperada.
Estimativas da Organização Mundial de Saúde sugerem que a prevalência de ansiedade em homens nas regiões globais estudadas deveria variar de 2,2% a 3,8%.
Na meta-análise, a taxa de ansiedade durante a gravidez foi de 9,9%, enquanto que durante o primeiro ano pós-parto foi de 11,7%.
Para chegar a esses números, os pesquisadores analisaram dados de 23 estudos, representando 40.124 participantes.
Resultados do estudo
O estudo demonstrou que o transtorno de ansiedade paterno apresenta prevalência significativa, com potencial impacto direto no apoio que o pai dá à mãe e ao bebê.
É fato que muitos homens aumentem seus níveis de ansiedade no período de transição para a paternidade. O nascimento de um filho ou uma filha é um evento muito importante na vida.
As mudanças que a paternidade traz influenciam emoções, relacionamentos, finanças e questões profissionais.
Portanto, buscar avaliação personalizada e conhecimento profissional especializado pode ser a chave para um bom prognóstico. Não há saúde sem saúde mental.
Referências
Leiferman, J. A., Farewell, C. V., Jewell, J., Lacy, R., Walls, J., Harnke, B., & Paulson, J. F. (2021). Anxiety among fathers during the prenatal and postpartum period: a meta-analysis. Journal of Psychosomatic Obstetrics & Gynecology, 1-10.
World Health Organization. (2017). Depression and other common mental disorders: global health estimates. World Health Organization.